ノーベル化学賞を受賞したリチウムイオン電池はどのような仕組み?

2019年、旭化成名誉フェローの吉野彰氏ら3人が、リチウムイオン電池の実用化への貢献を評価され、ノーベル化学賞を受賞しました。
スマホやタブレット、ノートPCなどの情報機器は、もはや私たちの生活に欠かせない道具です。
普段はあまり気にしていないかもしれませんが、実は携帯型の情報端末を動かすためには相当量の電力が必要で、長時間の利用ができるのもリチウムイオン電池と呼ばれる小型で軽い大容量電池のおかげなのです。
今回は、私たちの生活や仕事を一変させた大発明であるリチウムイオン電池の仕組みと生活や社会に与えたインパクトを解説します。
Contents [hide]
一次電池と二次電池の違いは?

私たちの生活に欠かせない存在となったリチウムイオン電池
私たちが日常的に使う電池にはさまざまな種類があります。
電力を生み出す仕組みや使われている素材も多様ですがおおまかには2種類で、放電のみが可能な使い捨ての「一次電池」と、充電して繰り返し使える「二次電池」に大別できます。
マンガン電池やアルカリ電池、水銀電池といった、一括りに乾電池とよばれるものが一次電池。
一方で、鉛蓄電池やリチウムイオン電池などが二次電池の代表例として挙げられます。
さて、これら多くの電池は「酸化」や「還元」といった化学反応を利用して電流を生み出しています。
電流は、電池の電極となる物質が他の物質に変化する際に、電荷を帯びた原子であるイオンを放出または吸収することで発生します。
そのため、電池のプラスとマイナスの電極に使う材料の組み合わせや、電極から電極へイオンを運ぶ電解液の種類によって、電池の特性が大きく変わります。
それに加えて、消費した電力を充電できる二次電池を作るためには化学変化で別のものに変えたり、戻したりできる電極の材料と電解液を選ばなければなりません。
その選定には以下の3つの要素で考える必要があります。
素材の耐久性
例えば、いったん鉄を酸化させて錆びさせると、還元して元のピカピカの鉄に戻すことは簡単ではありません。
しかも、包丁が錆びるとボロボロに刃こぼれするように、化学変化によって体積も変わるため、電極の形状が原形をとどめない場合も多くあります。
これでは、繰り返し利用することができません。
電極のダメージがわずかであっても電池が劣化していずれ使えなくなるため、なるべく電極のダメージが少ない材料を選ぶ必要があります。
素材から得られる電圧
中学校の理科で習ったように、電力は電圧と電流の掛け算で決まる値です。
このうち二次電池で得られる電圧の値は電極に使う素材の種類によって決まり、電流の値は主に電池のサイズで決まります。
単に大きな電力を得るだけならば、電池を大きくするだけで実現できますが、携帯性が犠牲となってしまいます。
つまり、使い勝手のよい電池を作るためには、より大きな電圧を生じる材料を選ぶ必要があるのです。
充放電にかかる時間や安全性
どんなに大容量の電池であっても、その充電時間が長かったのでは使い勝手がよくありません。
また、スマホゲームや動画視聴など、大きな電力を消費したいときにちびちびとしか放電できないのでは、大容量化した意味はないといえるでしょう。
さらに、充放電が一気にできる素材が見つかったとしても、安全性を損ねるような爆発的反応が起きるようなものは使えません。
短時間で充電し、一気に放電できる安全な二次電池を作るためには電極や電解液の材料選びと電極の形状が極めて重要です。
ノーベル賞につながった大発明、リチウムイオン電池はココがすごい
リチウムイオン電池では、一般に、正極材に「コバルト酸リチウム(LiCoO2)」を、負極材に黒鉛を、電解液には有機系の液体を使っています。
この材料の組み合わせを見つけ出し、電池として機能させるための原形を作ったのが、ノーベル化学賞を受賞した吉野章氏です。
吉野氏が発明した材料の組み合わせは、以下の4つの特長を持っています。
- 負極での化学反応が起きず、安全。
- 正極にコバルト酸リチウムを用いることで約4Vと高い起電力を得られる。
- 劣化が少なく、急速な充放電が可能で、蓄電状態を長期間安定的に保存できる。
- 利用する材料が空気中で安定しているため、電池の組み立てが容易。
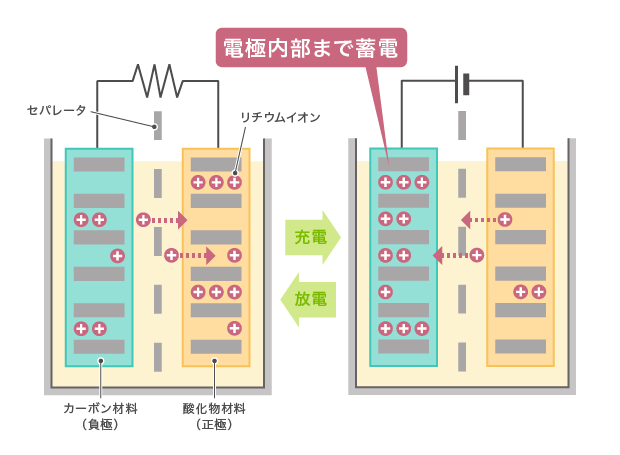
リチウムイオン電池が充放電する仕組み
二次電池としては、リチウムイオン電池以外にも、構成する材料が異なるニッケルカドミウム蓄電池、ニッケル水素電池、鉛蓄電池などがあります。
一定の体積当たりで蓄電可能な電力(体積エネルギー密度)と重量当たりで蓄電可能な電力(重量エネルギー密度)共に、リチウムイオン電池は圧倒的に優れているのです。
| 典型的な起電圧 | 典型的なエネルギー密度 | |
| リチウムイオン電池 | 3.7V | 201Wh/kg |
| ニッカド電池 | 1.2V | 39Wh/kg |
| ニッケル水素電池 | 1.2V | 61Wh/kg |
| 鉛蓄電池 | 12V | 40Wh/kg |
電池容量に関係する性能の比較
リチウムイオン電池の課題解決に向けた技術開発
数ある二次電池の中で傑出した特性を持つリチウムイオン電池ですが、改善すべき課題や伸びしろも残されています。
特に、これから急拡大する自動車向けバッテリーの性能と使い勝手の向上は喫緊の課題といえるでしょう。
リチウムイオン電池に限らず、二次電池には「過充電」と「過放電」というリスクを抱えています。
過充電とは、充電可能な電圧の限界(充電終止電圧)を超えた状態で充電し続けることです。
逆に、過放電とは放電可能な電圧の限界(放電終止電圧)を超えて放電し続けることを指します。
いずれも、電池の劣化や事故などにつながる可能性があり、終止電圧(安全に充放電を行える電圧の値のこと)になったらそれ以上充放電しないようにするシステム上の制御は欠かせません。
リチウムイオン電池の正極に使われるコバルト酸リチウムは、過放電や満充電の状態で放置しておくと劣化が早まる弱点がありました。
現在は、コバルト酸リチウムにニッケルとマンガンもしくはニッケルとアルミニウムを添加して安定性を高める技術が開発され、実用化しています。
さらに、現在のEV向けバッテリーは、最大容量の80%まで充電するのに、急速充電器を使っても約30分かかります。
これは、満タンまで5分足らずで終わるガソリン車の給油時間に比べると、かなり長い時間だといえるでしょう。
バッテリーの容量が少なく、航続距離が短い場合には頻繁な充電が必要となるため、充電時間の短時間化はEVの普及を大きく左右する課題です。
EV向けでは、バッテリーコストも課題です。
通常、リチウムイオン電池は、700回?800回充放電を繰り返すと劣化が一気に加速します。
ところが、リチウムイオン電池の電極に含まれるリチウムやコバルトは、いわゆるレアメタルであり原料費が高価であるため、現時点では、小型のEVでもバッテリーの交換に60万円強の費用がかかります。
これに対する解決策はまだ研究段階の技術ですが、電池内で電荷を運ぶ媒体をリチウムイオンから食塩にも含まれる安価なナトリウムイオンに変えたナトリウムイオン電池の開発が進められています。

電気自動車の普及はリチウムイオン電池の進化が鍵
究極のリチウムイオン電池、全固体電池
リチウムイオン電池の正極材料に空気、負極材料に金属リチウムを利用した場合、理論上ではエネルギー密度が既存品の10倍以上に向上することが知られています。
つまり、航続距離が400kmのEVを、バッテリーのサイズを変えずに4000km走るようにすることができるわけです。
ただし、その実現に向けたハードルは高く、その前段階として、特性向上につながる様々な電極材料が開発されており、リチウムイオン電池のエネルギー密度は年々高まっています。
これまでのリチウムイオン電池の有機溶媒には、発火しやすい揮発性の液体が使われていました。
これを固体の材料に変えることで、燃えにくく、液漏れもなく、両極の間で短絡することもないので、安全性を段違いに高められます。
この発展版のリチウムイオン電池は、「全固体電池」と呼ばれ、EV向けバッテリーの決定版と目されています。
安全性が高まった分、電極材料の選択の幅が広がり、より高性能化が可能になってきます。
EVの普及は、この全固体電池の実用化がカギを握っているのです。
ますます広がるリチウムイオン電池の用途
調査会社の富士経済は、世界のリチウムイオン電池の市場規模は2017年から2022年の5年間で2.3倍に成長し、7兆3914億円に達すると予測しています。
成長を引っ張る要因は、自動車です。
現在、世界中の自動車メーカーが、環境問題への対策の一環としてエンジンとモーターを併用するハイブリッド車(HEV)やモーターだけで動く電気自動車(EV)の開発を推し進めています。
特にEVでは、バッテリーの容量が連続航続距離を決めるため、大容量の二次電池が欠かせません。
こうした要求に応える時に電池として、リチウムイオン電池は他に代わるものがない優れた特性を持っています。
電源コンセントがないところでは使えなかったIT機器を持ち出して利用できるようになったのは、リチウムイオン電池が発明されたおかげです。
今後の応用範囲は、スマホやノートPCにとどまらず、生活や仕事、そして社会の仕組みまで変えていくことでしょう。


